Bonjour, je m’appelle Minh, et suis anesthésiste-réanimateur.
Rémi m’a invité ici pour discuter de la noradrénaline en anesthésie.
Les agents anesthésiques couramment utilisés induisent une sympatholyse, une diminution de la noradrénaline et de l’adrénaline endogènes, résultant en une veinodilatation responsable d’une baisse de la précharge, et donc du débit cardiaque. Sur nos moniteurs, nous voyons souvent une hypotension artérielle apparaître, reflet de cette baisse du débit cardiaque.
Plusieurs solutions s’offrent à nous pour restaurer ce débit cardiaque.

Nous pouvons remplir le contenu veineux. Le contenant étant plus volumineux, la restauration de la précharge sera longue par cette méthode. Il y aura donc un temps d’hypodébit cardiaque et donc d’hypoperfusion d’organe assez long.
Le bon sens nous dirait : nous avons veinodilaté, il nous suffit donc de veinoconstricter.
Veinoconstrictons. Et nous avons des produits pour ça : éphédrine (E), néosynéphrine (N), noradrénaline (NA).
L’E agit par un mécanisme majoritairement indirect, en libérant les cathécholamines endogènes au niveau des terminaisons nerveuses. Elle augmente donc la noradrénaline endogène, favorisant la veinoconstriction et l’augmentation du débit cardiaque. Par ailleurs, elle induit une tachycardie.
En pratique, elle fonctionne, mais son efficacité est aléatoire, et épuisable.
Chez un patient que l’on ne veut pas rendre tachycarde, elle peut être délétère.
La N, de part son activité alpha1, a une activité purement vasoconstrictrice : veinoconstrictrice et artérioconstrictrice. Après administration de N, la pression artérielle remonte. Nous sommes contents. Cependant, le débit cardiaque diminue. Rappelons que PA = Q * RVS, ou PA est la pression artérielle, Q le débit cardiaque, RVS les résistances vasculaires systémiques. N augmente les RVS, mais diminue le Q, car augmente la postcharge. Le ventricule gauche (VG) doit lutter contre une postcharge plus importante, et chez les patients aux antécédents de dysfonction VG, la N peut suraltérer la fonction VG.
La NA est un vasoconstricteur. Veinoconstricteur en grande partie, et aussi un peu artérioconstricteur. Une administration de NA entraine une augmentation de la précharge, très peu de la postcharge, et en résulte une augmentation du débit cardiaque. C’est exactement ce que nous cherchons à faire. Nous savons que les agents anesthésiques couramment utilisés induisent une sympatholyse, une diminution de la noradrénaline et de l’adrénaline endogènes, résultant en une veinodilatation responsable d’une baisse de la précharge, et donc du débit cardiaque. La NA semble être la drogue de choix.
Alors pourquoi ne l’utilisons-nous pas ? Juste personnellement, je pense qu’une non utilisation de la NA ne peut relever que d’une méconnaissance de ce médicament. J’ai souvent entendu :
“Ca fait trop de vasoconstriction, il va faire un infartcus” -> Si on dit “trop”, c’est qu’il y a un effet dose. Il faut donc diminuer les doses. Et la NA n’est pas plus artérioconstrictrice que la N.
“J’ai déjà vu des gens amputés des 4 membres car trop de NA” -> C’était probablement des chocs septiques, avec une coagulopathie septique, des microthrombi, une défaillance endothéliale, nécéssitant des fortes doses de NA pour survivre. Certes, il y a eu une nécrose des extrémités, mais réfléchissons : imaginons que cette nécrose serait dûe à la NA. Imputabilité de la NA ? Arrêtons donc la NA. Les extrémités ne deviendraient pas roses, ce serait même plutôt tout l’organisme qui serait nécrosé.
« Moi j’ai toujours fait de la néo, ça a toujours marché » -> Effectivement si la finalité est la pression artérielle (mesurée dans les gros troncs artériels), la néo marche. Mais aujourd’hui, où notre finalité est le débit cardiaque, ben ça ne marche plus…
On administre du blanc, on diminue le débit cardiaque, on hypoperfuse les organes. On trouve ça normal.
Pourquoi ne pas antagoniser notre iatrogénie ?
C’est comme si je renversais du café dans la salle de pause, et que je disais “ça va sècher” ou “l’ASH va le faire”. Vous trouvez ça normal ?
Et du coup, la NA, c’est bien, mais est-ce qu’on a du recul là-dessus ?
La réponse est oui.
Une étude randomisée comparant la N et la NA chez des patientes bénéficiant d’une césarienne sous rachianesthésie publiée dans Anesthesiology en 2015 retrouvait : meilleur débit cardiaque dans le groupe NA, pas de différence de l’Apgar, meilleur pH néonatal dans le groupe NA, et, étonnamment, les dosages de noradrénaline et d’adrénaline dans l’artère et la veine ombilicales revenaient plus hauts dans le groupe N que dans le groupe NA. Adaptation foetale à l’hypoperfusion utéroplacentaire ?.
D’autres travaux comparant N et NA retrouvent une diminution du débit cardiaque dans le groupe N (voir table ci-dessous, extraite d’un article en accès libre).

En pratique : voici une recette que je trouve facile et efficace :
Une ampoule de NA (8mg) dans NaCl 0,9% ou SG5% 500mL = 16µg/mL.
A l’induction, tout de suite après avoir poussé l’agent hypodynamisant : 8µg (0,5mL) à 32µg (2mL) en bolus selon fragilité prévisible du patient.
Si nécessité de répéter les boli : seringue autopulsée, environ 30mL/h, à adapter selon la cinétique du débit cardiaque ou de la pression artérielle.
Une fois après avoir essayé, on ne peut plus s’en passer.
En plus, c’est tout doux.
Ca marche au bloc, mais c’est aussi une aide précieuse en réa ou dans les étages quand on est amené à intuber dans l’urgence.
En conclusion :
L’induction anesthésique s’accompagne le plus souvent d’une diminution du débit cardiaque, dont les mécanismes font intervenir une sympatholyse, une diminution de la noradrénaline et de l’adrénaline endogènes, résultant en une veinodilatation responsable d’une baisse de la précharge, et donc du débit cardiaque.
La noradrénaline antagonise ces mêmes mécanismes et restaure efficacement le débit cardiaque.
Pour une lecture plus approfondie, je vous propose:
Mets B. Should Norepinephrine, Rather than Phenylephrine, Be Considered the Primary Vasopressor in Anesthetic Practice? Anesth Analg 2016 May;122(5):1707-14.
Merci de votre attention.
Minh
(Je peux mettre à jour le billet de recette face à une hypotension ?!)
UPDATE : Beau travail du Pr FUTIER http://jamanetwork.com/journals/jama/fullarticle/2654895
UPDATE par Rémi/nfkb :
L’utilisation de la noradrénaline plus précocement est intéressante comme le montre Minh içi et notre pratique tant à le prouver. Néanmoins, ce médicament très puissant reste à manier dans des environnements adaptés et penser à switcher vite vers des concentrations plus élevées et à monitorer la pression artérielle de façon invasive dès que le patient devient instable et pas juste un peu vasoplégique à cause des drogues d’anesthésie. Merci Grégoire.
Update #2 Au quotidien, nous avons protocolé son utilisation dans le service avec une dilution dans une poche (Baxter Mono-luer) qui ne se percute pour éviter l’erreur d’administrer la poche en débit libre à un patient (merci Benjamin).
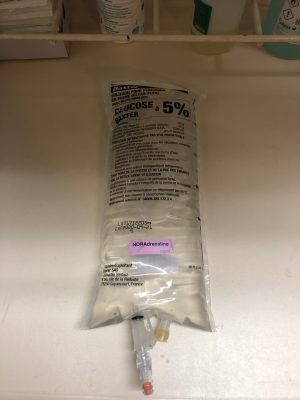 Cette poche reste dans un endroit précis. De plus, j’ai plutôt tendance à faire de plus en plus de SAP. Les boli je les limite à 16 µg, quitte à les répéter (après un résultat de PNI) en attendant l’introduction de la SAP. Je me focalise sur les patients les plus âgés ou fragiles. La noradrénaline en bolus à un patient jeune, ASA 1, vierge de médicaments au long cours (anti-HTA, antidépresseurs, etc) me parait plus sujette à des réactions importantes. Autour de 30/40 ml/h, il faut réfléchir à la situation et il parait logique de préparer de la noradrénaline plus concentrée en SAP.
Cette poche reste dans un endroit précis. De plus, j’ai plutôt tendance à faire de plus en plus de SAP. Les boli je les limite à 16 µg, quitte à les répéter (après un résultat de PNI) en attendant l’introduction de la SAP. Je me focalise sur les patients les plus âgés ou fragiles. La noradrénaline en bolus à un patient jeune, ASA 1, vierge de médicaments au long cours (anti-HTA, antidépresseurs, etc) me parait plus sujette à des réactions importantes. Autour de 30/40 ml/h, il faut réfléchir à la situation et il parait logique de préparer de la noradrénaline plus concentrée en SAP.
{858234:2P7XKMMT},{858234:FJINQZDK};{858234:THWXH8FF};{858234:W72XQKSW},{858234:ETN93IU5};{858234:HQVBBA3F};{858234:ETN93IU5},{858234:HQVBBA3F};{858234:7AZ5WMS3};{858234:F5JMT8H2};{858234:F5JMT8H2}
default
asc
no
1
7504
%7B%22status%22%3A%22success%22%2C%22updateneeded%22%3Afalse%2C%22instance%22%3A%22zotpress-36c682fc237c61a74d86ad7a6fcb5925%22%2C%22meta%22%3A%7B%22request_last%22%3A0%2C%22request_next%22%3A0%2C%22used_cache%22%3Atrue%7D%2C%22data%22%3A%5B%7B%22key%22%3A%22F5JMT8H2%22%2C%22library%22%3A%7B%22id%22%3A858234%7D%2C%22meta%22%3A%7B%22creatorSummary%22%3A%22Mets%22%2C%22parsedDate%22%3A%222016-05%22%2C%22numChildren%22%3A1%7D%2C%22bib%22%3A%22%3Cdiv%20class%3D%5C%22csl-bib-body%5C%22%20style%3D%5C%22line-height%3A%201.35%3B%20%5C%22%3E%5Cn%20%20%3Cdiv%20class%3D%5C%22csl-entry%5C%22%20style%3D%5C%22clear%3A%20left%3B%20%5C%22%3E%5Cn%20%20%20%20%3Cdiv%20class%3D%5C%22csl-left-margin%5C%22%20style%3D%5C%22float%3A%20left%3B%20padding-right%3A%200.5em%3B%20text-align%3A%20right%3B%20width%3A%201em%3B%5C%22%3E1.%3C%5C%2Fdiv%3E%3Cdiv%20class%3D%5C%22csl-right-inline%5C%22%20style%3D%5C%22margin%3A%200%20.4em%200%201.5em%3B%5C%22%3EMets%20B.%20Should%20Norepinephrine%2C%20Rather%20than%20Phenylephrine%2C%20Be%20Considered%20the%20Primary%20Vasopressor%20in%20Anesthetic%20Practice%3F%20Anesth%20Analg.%202016%20May%3B122%285%29%3A1707%26%23x2013%3B14.%3C%5C%2Fdiv%3E%5Cn%20%20%20%3C%5C%2Fdiv%3E%5Cn%3C%5C%2Fdiv%3E%22%2C%22data%22%3A%7B%22itemType%22%3A%22journalArticle%22%2C%22title%22%3A%22Should%20Norepinephrine%2C%20Rather%20than%20Phenylephrine%2C%20Be%20Considered%20the%20Primary%20Vasopressor%20in%20Anesthetic%20Practice%3F%22%2C%22creators%22%3A%5B%7B%22creatorType%22%3A%22author%22%2C%22firstName%22%3A%22Berend%22%2C%22lastName%22%3A%22Mets%22%7D%5D%2C%22abstractNote%22%3A%22%22%2C%22date%22%3A%22May%202016%22%2C%22language%22%3A%22eng%22%2C%22DOI%22%3A%2210.1213%5C%2FANE.0000000000001239%22%2C%22ISSN%22%3A%221526-7598%22%2C%22url%22%3A%22%22%2C%22collections%22%3A%5B%228BC4ZE5V%22%5D%2C%22dateModified%22%3A%222017-08-07T06%3A39%3A35Z%22%7D%7D%2C%7B%22key%22%3A%227AZ5WMS3%22%2C%22library%22%3A%7B%22id%22%3A858234%7D%2C%22meta%22%3A%7B%22creatorSummary%22%3A%22Ngan%20Kee%20et%20al.%22%2C%22parsedDate%22%3A%222015-04%22%2C%22numChildren%22%3A1%7D%2C%22bib%22%3A%22%3Cdiv%20class%3D%5C%22csl-bib-body%5C%22%20style%3D%5C%22line-height%3A%201.35%3B%20%5C%22%3E%5Cn%20%20%3Cdiv%20class%3D%5C%22csl-entry%5C%22%20style%3D%5C%22clear%3A%20left%3B%20%5C%22%3E%5Cn%20%20%20%20%3Cdiv%20class%3D%5C%22csl-left-margin%5C%22%20style%3D%5C%22float%3A%20left%3B%20padding-right%3A%200.5em%3B%20text-align%3A%20right%3B%20width%3A%201em%3B%5C%22%3E1.%3C%5C%2Fdiv%3E%3Cdiv%20class%3D%5C%22csl-right-inline%5C%22%20style%3D%5C%22margin%3A%200%20.4em%200%201.5em%3B%5C%22%3ENgan%20Kee%20WD%2C%20Lee%20SWY%2C%20Ng%20FF%2C%20Tan%20PE%2C%20Khaw%20KS.%20Randomized%20double-blinded%20comparison%20of%20norepinephrine%20and%20phenylephrine%20for%20maintenance%20of%20blood%20pressure%20during%20spinal%20anesthesia%20for%20cesarean%20delivery.%20Anesthesiology.%202015%20Apr%3B122%284%29%3A736%26%23x2013%3B45.%3C%5C%2Fdiv%3E%5Cn%20%20%20%3C%5C%2Fdiv%3E%5Cn%3C%5C%2Fdiv%3E%22%2C%22data%22%3A%7B%22itemType%22%3A%22journalArticle%22%2C%22title%22%3A%22Randomized%20double-blinded%20comparison%20of%20norepinephrine%20and%20phenylephrine%20for%20maintenance%20of%20blood%20pressure%20during%20spinal%20anesthesia%20for%20cesarean%20delivery%22%2C%22creators%22%3A%5B%7B%22creatorType%22%3A%22author%22%2C%22firstName%22%3A%22Warwick%20D.%22%2C%22lastName%22%3A%22Ngan%20Kee%22%7D%2C%7B%22creatorType%22%3A%22author%22%2C%22firstName%22%3A%22Shara%20W.%20Y.%22%2C%22lastName%22%3A%22Lee%22%7D%2C%7B%22creatorType%22%3A%22author%22%2C%22firstName%22%3A%22Floria%20F.%22%2C%22lastName%22%3A%22Ng%22%7D%2C%7B%22creatorType%22%3A%22author%22%2C%22firstName%22%3A%22Perpetua%20E.%22%2C%22lastName%22%3A%22Tan%22%7D%2C%7B%22creatorType%22%3A%22author%22%2C%22firstName%22%3A%22Kim%20S.%22%2C%22lastName%22%3A%22Khaw%22%7D%5D%2C%22abstractNote%22%3A%22BACKGROUND%3A%20During%20spinal%20anesthesia%20for%20cesarean%20delivery%2C%20phenylephrine%20can%20cause%20reflexive%20decreases%20in%20maternal%20heart%20rate%20and%20cardiac%20output.%20Norepinephrine%20has%20weak%20%5Cu03b2-adrenergic%20receptor%20agonist%20activity%20in%20addition%20to%20potent%20%5Cu03b1-adrenergic%20receptor%20activity%20and%20therefore%20may%20be%20suitable%20for%20maintaining%20blood%20pressure%20with%20less%20negative%20effects%20on%20heart%20rate%20and%20cardiac%20output%20compared%20with%20phenylephrine.%5CnMETHODS%3A%20In%20a%20randomized%2C%20double-blinded%20study%2C%20104%20healthy%20patients%20having%20cesarean%20delivery%20under%20spinal%20anesthesia%20were%20randomized%20to%20have%20systolic%20blood%20pressure%20maintained%20with%20a%20computer-controlled%20infusion%20of%20norepinephrine%205%20%5Cu03bcg%5C%2Fml%20or%20phenylephrine%20100%20%5Cu03bcg%5C%2Fml.%20The%20primary%20outcome%20compared%20was%20cardiac%20output.%20Blood%20pressure%20heart%20rate%20and%20neonatal%20outcome%20were%20also%20compared.%5CnRESULTS%3A%20Normalized%20cardiac%20output%205%20min%20after%20induction%20was%20greater%20in%20the%20norepinephrine%20group%20versus%20the%20phenylephrine%20group%20%28median%20102.7%25%20%5Binterquartile%20range%2C%2094.3%20to%20116.7%25%5D%20versus%2093.8%25%20%5B85.0%20to%20103.1%25%5D%2C%20P%20%3D%200.004%2C%20median%20difference%209.8%25%2C%2095%25%20CI%20of%20difference%20between%20medians%202.8%20to%2016.1%25%29.%20From%20induction%20until%20uterine%20incision%2C%20for%20norepinephrine%20versus%20phenylephrine%2C%20systolic%20blood%20pressure%20and%20stroke%20volume%20were%20similar%2C%20heart%20rate%20and%20cardiac%20output%20were%20greater%2C%20systemic%20vascular%20resistance%20was%20lower%2C%20and%20the%20incidence%20of%20bradycardia%20was%20smaller.%20Neonatal%20outcome%20was%20similar%20between%20groups.%5CnCONCLUSIONS%3A%20When%20given%20by%20computer-controlled%20infusion%20during%20spinal%20anesthesia%20for%20cesarean%20delivery%2C%20norepinephrine%20was%20effective%20for%20maintaining%20blood%20pressure%20and%20was%20associated%20with%20greater%20heart%20rate%20and%20cardiac%20output%20compared%20with%20phenylephrine.%20Further%20work%20would%20be%20of%20interest%20to%20confirm%20the%20safety%20and%20efficacy%20of%20norepinephrine%20as%20a%20vasopressor%20in%20obstetric%20patients.%22%2C%22date%22%3A%22Apr%202015%22%2C%22language%22%3A%22eng%22%2C%22DOI%22%3A%2210.1097%5C%2FALN.0000000000000601%22%2C%22ISSN%22%3A%221528-1175%22%2C%22url%22%3A%22%22%2C%22collections%22%3A%5B%228BC4ZE5V%22%5D%2C%22dateModified%22%3A%222017-08-07T06%3A39%3A10Z%22%7D%7D%2C%7B%22key%22%3A%22HQVBBA3F%22%2C%22library%22%3A%7B%22id%22%3A858234%7D%2C%22meta%22%3A%7B%22creatorSummary%22%3A%22DiNardo%20and%20Zvara%22%2C%22parsedDate%22%3A%222008-04-15%22%2C%22numChildren%22%3A1%7D%2C%22bib%22%3A%22%3Cdiv%20class%3D%5C%22csl-bib-body%5C%22%20style%3D%5C%22line-height%3A%201.35%3B%20%5C%22%3E%5Cn%20%20%3Cdiv%20class%3D%5C%22csl-entry%5C%22%20style%3D%5C%22clear%3A%20left%3B%20%5C%22%3E%5Cn%20%20%20%20%3Cdiv%20class%3D%5C%22csl-left-margin%5C%22%20style%3D%5C%22float%3A%20left%3B%20padding-right%3A%200.5em%3B%20text-align%3A%20right%3B%20width%3A%201em%3B%5C%22%3E1.%3C%5C%2Fdiv%3E%3Cdiv%20class%3D%5C%22csl-right-inline%5C%22%20style%3D%5C%22margin%3A%200%20.4em%200%201.5em%3B%5C%22%3EDiNardo%20JA%2C%20Zvara%20DA.%20Anesthesia%20for%20Cardiac%20Surgery.%20John%20Wiley%20%26amp%3B%20Sons%3B%202008.%20475%20p.%3C%5C%2Fdiv%3E%5Cn%20%20%20%3C%5C%2Fdiv%3E%5Cn%3C%5C%2Fdiv%3E%22%2C%22data%22%3A%7B%22itemType%22%3A%22book%22%2C%22title%22%3A%22Anesthesia%20for%20Cardiac%20Surgery%22%2C%22creators%22%3A%5B%7B%22creatorType%22%3A%22author%22%2C%22firstName%22%3A%22James%20A.%22%2C%22lastName%22%3A%22DiNardo%22%7D%2C%7B%22creatorType%22%3A%22author%22%2C%22firstName%22%3A%22David%20A.%22%2C%22lastName%22%3A%22Zvara%22%7D%5D%2C%22abstractNote%22%3A%22This%20comprehensive%2C%20state%20of%20the%20art%20overview%20of%20pediatric%20and%20adult%20cardiac%20anesthesia%20brings%20together%20all%20the%20latest%20developments%20in%20this%20rapidly%20developing%20field.%20This%20text%20is%20intended%20both%20as%20a%20reference%20and%20for%20daily%20use%20by%20practicing%20and%20prospective%20anesthesiologists.%20Thoroughly%20updated%20for%20its%20third%20edition%2C%20Anesthesia%20for%20Cardiac%20Surgery%20fills%20the%20gap%20between%20encyclopaedic%20references%20and%20brief%20outlines%2C%20presenting%20just%20the%20right%20amount%20of%20information%20to%20guide%20trainees%20and%20practitioners%20who%20care%20for%20cardiac%20surgical%20patients.%20This%20edition%20features%3A%20%20The%20introduction%20of%20Dr%20Zvara%20as%20co-editor%20A%20new%20chapter%20on%20Special%20Considerations%20Practical%20clinical%20information%20coupled%20with%20comprehensive%20descriptions%20of%20physiology%20Key%20facts%20and%20tables%20summarized%20for%20convenient%20access%20%20This%20essential%20resource%20will%20prove%20invaluable%20for%20residents%2C%20fellows%2C%20and%20practicing%20anesthesiologists.%22%2C%22date%22%3A%222008-04-15%22%2C%22language%22%3A%22en%22%2C%22ISBN%22%3A%229780470765920%22%2C%22url%22%3A%22%22%2C%22collections%22%3A%5B%228BC4ZE5V%22%5D%2C%22dateModified%22%3A%222017-08-07T06%3A38%3A50Z%22%7D%7D%2C%7B%22key%22%3A%22ETN93IU5%22%2C%22library%22%3A%7B%22id%22%3A858234%7D%2C%22meta%22%3A%7B%22creatorSummary%22%3A%22Magder%22%2C%22parsedDate%22%3A%222011-08%22%2C%22numChildren%22%3A1%7D%2C%22bib%22%3A%22%3Cdiv%20class%3D%5C%22csl-bib-body%5C%22%20style%3D%5C%22line-height%3A%201.35%3B%20%5C%22%3E%5Cn%20%20%3Cdiv%20class%3D%5C%22csl-entry%5C%22%20style%3D%5C%22clear%3A%20left%3B%20%5C%22%3E%5Cn%20%20%20%20%3Cdiv%20class%3D%5C%22csl-left-margin%5C%22%20style%3D%5C%22float%3A%20left%3B%20padding-right%3A%200.5em%3B%20text-align%3A%20right%3B%20width%3A%201em%3B%5C%22%3E1.%3C%5C%2Fdiv%3E%3Cdiv%20class%3D%5C%22csl-right-inline%5C%22%20style%3D%5C%22margin%3A%200%20.4em%200%201.5em%3B%5C%22%3EMagder%20S.%20Phenylephrine%20and%20tangible%20bias.%20Anesth%20Analg.%202011%20Aug%3B113%282%29%3A211%26%23x2013%3B3.%3C%5C%2Fdiv%3E%5Cn%20%20%20%3C%5C%2Fdiv%3E%5Cn%3C%5C%2Fdiv%3E%22%2C%22data%22%3A%7B%22itemType%22%3A%22journalArticle%22%2C%22title%22%3A%22Phenylephrine%20and%20tangible%20bias%22%2C%22creators%22%3A%5B%7B%22creatorType%22%3A%22author%22%2C%22firstName%22%3A%22Sheldon%22%2C%22lastName%22%3A%22Magder%22%7D%5D%2C%22abstractNote%22%3A%22%22%2C%22date%22%3A%22Aug%202011%22%2C%22language%22%3A%22eng%22%2C%22DOI%22%3A%2210.1213%5C%2FANE.0b013e318220406a%22%2C%22ISSN%22%3A%221526-7598%22%2C%22url%22%3A%22%22%2C%22collections%22%3A%5B%228BC4ZE5V%22%5D%2C%22dateModified%22%3A%222017-08-07T06%3A38%3A09Z%22%7D%7D%2C%7B%22key%22%3A%22W72XQKSW%22%2C%22library%22%3A%7B%22id%22%3A858234%7D%2C%22meta%22%3A%7B%22creatorSummary%22%3A%22Thiele%20et%20al.%22%2C%22parsedDate%22%3A%222011-08%22%2C%22numChildren%22%3A1%7D%2C%22bib%22%3A%22%3Cdiv%20class%3D%5C%22csl-bib-body%5C%22%20style%3D%5C%22line-height%3A%201.35%3B%20%5C%22%3E%5Cn%20%20%3Cdiv%20class%3D%5C%22csl-entry%5C%22%20style%3D%5C%22clear%3A%20left%3B%20%5C%22%3E%5Cn%20%20%20%20%3Cdiv%20class%3D%5C%22csl-left-margin%5C%22%20style%3D%5C%22float%3A%20left%3B%20padding-right%3A%200.5em%3B%20text-align%3A%20right%3B%20width%3A%201em%3B%5C%22%3E1.%3C%5C%2Fdiv%3E%3Cdiv%20class%3D%5C%22csl-right-inline%5C%22%20style%3D%5C%22margin%3A%200%20.4em%200%201.5em%3B%5C%22%3EThiele%20RH%2C%20Nemergut%20EC%2C%20Lynch%20C.%20The%20clinical%20implications%20of%20isolated%20alpha%281%29%20adrenergic%20stimulation.%20Anesth%20Analg.%202011%20Aug%3B113%282%29%3A297%26%23x2013%3B304.%3C%5C%2Fdiv%3E%5Cn%20%20%20%3C%5C%2Fdiv%3E%5Cn%3C%5C%2Fdiv%3E%22%2C%22data%22%3A%7B%22itemType%22%3A%22journalArticle%22%2C%22title%22%3A%22The%20clinical%20implications%20of%20isolated%20alpha%281%29%20adrenergic%20stimulation%22%2C%22creators%22%3A%5B%7B%22creatorType%22%3A%22author%22%2C%22firstName%22%3A%22Robert%20H.%22%2C%22lastName%22%3A%22Thiele%22%7D%2C%7B%22creatorType%22%3A%22author%22%2C%22firstName%22%3A%22Edward%20C.%22%2C%22lastName%22%3A%22Nemergut%22%7D%2C%7B%22creatorType%22%3A%22author%22%2C%22firstName%22%3A%22Carl%22%2C%22lastName%22%3A%22Lynch%22%7D%5D%2C%22abstractNote%22%3A%22Phenylephrine%20is%20a%20direct-acting%2C%20predominantly%20%5Cu03b1%281%29%20adrenergic%20receptor%20agonist%20used%20by%20anesthesiologists%20and%20intensivists%20to%20treat%20hypotension.%20A%20variety%20of%20physiologic%20studies%20suggest%20that%20%5Cu03b1-agonists%20increase%20cardiac%20afterload%2C%20reduce%20venous%20compliance%2C%20and%20reduce%20renal%20bloodflow.%20The%20effects%20on%20gastrointestinal%20and%20cerebral%20perfusion%20are%20controversial.%20To%20better%20understand%20the%20effects%20of%20phenylephrine%20in%20a%20variety%20of%20clinical%20settings%2C%20we%20screened%20463%20articles%20on%20the%20basis%20of%20PubMed%20searches%20of%20%5C%22methoxamine%2C%5C%22%20a%20long-acting%20%5Cu03b1%20agonist%2C%20and%20%5C%22phenylephrine%5C%22%20%28limited%20to%20human%2C%20randomized%20studies%20published%20in%20English%29%2C%20as%20well%20as%20citations%20found%20therein.%20Relevant%20articles%2C%20as%20well%20as%20those%20discovered%20in%20the%20peer-review%20process%2C%20were%20incorporated%20into%20this%20review.%20Phenylephrine%20has%20been%20studied%20as%20an%20antihypotensive%20drug%20in%20patients%20with%20severe%20aortic%20stenosis%2C%20as%20a%20treatment%20for%20decompensated%20tetralogy%20of%20Fallot%20and%20hypoxemia%20during%201-lung%20ventilation%2C%20as%20well%20as%20for%20the%20treatment%20of%20septic%20shock%2C%20traumatic%20brain%20injury%2C%20vasospasm%20status-postsubarachnoid%20hemorrhage%2C%20and%20hypotension%20during%20cesarean%20delivery.%20In%20specific%20instances%20%28critical%20aortic%20stenosis%2C%20tetralogy%20of%20Fallot%2C%20hypotension%20during%20cesarean%20delivery%29%20in%20which%20the%20regional%20effects%20of%20phenylephrine%20%28e.g.%2C%20decreased%20heart%20rate%2C%20favorable%20alterations%20in%20Q%28p%29%3AQ%28s%29%20ratio%2C%20improved%20fetal%20oxygen%20supply%3Ademand%20ratio%29%20outweigh%20its%20global%20effects%20%28e.g.%2C%20decreased%20cardiac%20output%29%2C%20phenylephrine%20may%20be%20a%20rational%20pharmacologic%20choice.%20In%20pathophysiologic%20states%20in%20which%20no%20regional%20advantages%20are%20gained%20by%20using%20an%20%5Cu03b1%281%29%20agonist%2C%20alternative%20vasopressors%20should%20be%20sought.%22%2C%22date%22%3A%22Aug%202011%22%2C%22language%22%3A%22eng%22%2C%22DOI%22%3A%2210.1213%5C%2FANE.0b013e3182120ca5%22%2C%22ISSN%22%3A%221526-7598%22%2C%22url%22%3A%22%22%2C%22collections%22%3A%5B%228BC4ZE5V%22%5D%2C%22dateModified%22%3A%222017-08-07T06%3A37%3A50Z%22%7D%7D%2C%7B%22key%22%3A%22THWXH8FF%22%2C%22library%22%3A%7B%22id%22%3A858234%7D%2C%22meta%22%3A%7B%22creatorSummary%22%3A%22Kanaya%20et%20al.%22%2C%22parsedDate%22%3A%222002-05%22%2C%22numChildren%22%3A1%7D%2C%22bib%22%3A%22%3Cdiv%20class%3D%5C%22csl-bib-body%5C%22%20style%3D%5C%22line-height%3A%201.35%3B%20%5C%22%3E%5Cn%20%20%3Cdiv%20class%3D%5C%22csl-entry%5C%22%20style%3D%5C%22clear%3A%20left%3B%20%5C%22%3E%5Cn%20%20%20%20%3Cdiv%20class%3D%5C%22csl-left-margin%5C%22%20style%3D%5C%22float%3A%20left%3B%20padding-right%3A%200.5em%3B%20text-align%3A%20right%3B%20width%3A%201em%3B%5C%22%3E1.%3C%5C%2Fdiv%3E%3Cdiv%20class%3D%5C%22csl-right-inline%5C%22%20style%3D%5C%22margin%3A%200%20.4em%200%201.5em%3B%5C%22%3EKanaya%20N%2C%20Satoh%20H%2C%20Seki%20S%2C%20Nakayama%20M%2C%20Namiki%20A.%20Propofol%20anesthesia%20enhances%20the%20pressor%20response%20to%20intravenous%20ephedrine.%20Anesth%20Analg.%202002%20May%3B94%285%29%3A1207%26%23x2013%3B11%2C%20table%20of%20contents.%3C%5C%2Fdiv%3E%5Cn%20%20%20%3C%5C%2Fdiv%3E%5Cn%3C%5C%2Fdiv%3E%22%2C%22data%22%3A%7B%22itemType%22%3A%22journalArticle%22%2C%22title%22%3A%22Propofol%20anesthesia%20enhances%20the%20pressor%20response%20to%20intravenous%20ephedrine%22%2C%22creators%22%3A%5B%7B%22creatorType%22%3A%22author%22%2C%22firstName%22%3A%22Noriaki%22%2C%22lastName%22%3A%22Kanaya%22%7D%2C%7B%22creatorType%22%3A%22author%22%2C%22firstName%22%3A%22Hitoshi%22%2C%22lastName%22%3A%22Satoh%22%7D%2C%7B%22creatorType%22%3A%22author%22%2C%22firstName%22%3A%22Sumihiko%22%2C%22lastName%22%3A%22Seki%22%7D%2C%7B%22creatorType%22%3A%22author%22%2C%22firstName%22%3A%22Masayasu%22%2C%22lastName%22%3A%22Nakayama%22%7D%2C%7B%22creatorType%22%3A%22author%22%2C%22firstName%22%3A%22Akiyoshi%22%2C%22lastName%22%3A%22Namiki%22%7D%5D%2C%22abstractNote%22%3A%22The%20induction%20of%20anesthesia%20with%20propofol%20is%20often%20associated%20with%20a%20decrease%20in%20arterial%20blood%20pressure%20%28BP%29.%20Although%20vasopressors%20are%20sometimes%20required%20to%20reverse%20the%20propofol-induced%20hypotension%2C%20little%20is%20known%20about%20the%20effect%20of%20propofol%20on%20these%20drugs.%20We%20studied%20the%20effects%20of%20propofol%20and%20sevoflurane%20on%20pressor%20response%20to%20i.v.%20ephedrine.%20Thirty%20adult%20patients%20were%20randomly%20assigned%20to%20one%20of%20two%20groups.%20In%20the%20Propofol%20group%20%28n%20%3D%2015%29%2C%20patients%20received%20propofol%202.5%20mg%5C%2Fkg%20i.v.%20for%20induction%20followed%20by%20100%20microg%20x%20kg%28-1%29%20x%20min%28-1%29%20i.v.%20for%20maintenance.%20In%20the%20Sevoflurane%20group%20%28n%20%3D%2015%29%2C%20anesthesia%20was%20induced%20with%20sevoflurane%203%25-4%25%20in%20oxygen%20and%20maintained%20with%20sevoflurane%202%25%20in%20oxygen.%20All%20patients%20in%20both%20groups%20received%20ephedrine%200.1%20mg%5C%2Fkg%20i.v.%20before%20and%20after%20the%20anesthetic%20induction.%20Ephedrine%20increased%20the%20heart%20rate%20significantly%20%28P%20%3C%200.05%29%20in%20awake%20patients%20in%20both%20study%20groups.%20In%20contrast%2C%20there%20was%20no%20increase%20in%20heart%20rate%20after%20the%20ephedrine%20administration%20under%20propofol%20or%20sevoflurane%20anesthesia.%20In%20awake%20patients%2C%20transient%20increases%20in%20mean%20BP%20were%20observed%20after%20i.v.%20ephedrine%20in%20both%20groups.%20In%20the%20Propofol%20group%2C%202%20min%20after%20the%20administration%20of%20ephedrine%2C%20mean%20BP%20increased%2016%25%20%2B%5C%2F-%2010%25%20under%20anesthesia%20but%20increased%20only%204%25%20%2B%5C%2F-%206%25%20when%20the%20same%20patients%20were%20awake.%20The%20magnitudes%20of%20the%20pressor%20responses%20to%20ephedrine%20during%20propofol%20anesthesia%20were%20significantly%20greater%20%28P%20%3C%200.05%29%20than%20during%20the%20awake%20state.%20However%2C%20ephedrine%200.1%20mg%5C%2Fkg%20i.v.%20showed%20no%20significant%20increases%20in%20BP%20during%20sevoflurane%20anesthesia.%20We%20conclude%20that%20propofol%2C%20not%20sevoflurane%2C%20anesthesia%20augments%20the%20pressor%20responses%20to%20i.v.%20ephedrine.%5CnIMPLICATIONS%3A%20The%20effect%20of%20anesthetics%20on%20vasopressor-mediated%20cardiovascular%20effects%20is%20poorly%20understood.%20We%20evaluated%20the%20pressor%20response%20to%20ephedrine%20during%20propofol%20or%20sevoflurane%20anesthesia.%20Our%20study%20suggests%20that%20anesthesia-induced%20hypotension%20may%20be%20easier%20to%20reverse%20with%20ephedrine%20during%20propofol%20anesthesia%20than%20during%20sevoflurane%20anesthesia.%22%2C%22date%22%3A%22May%202002%22%2C%22language%22%3A%22eng%22%2C%22DOI%22%3A%22%22%2C%22ISSN%22%3A%220003-2999%22%2C%22url%22%3A%22%22%2C%22collections%22%3A%5B%228BC4ZE5V%22%5D%2C%22dateModified%22%3A%222017-08-07T06%3A37%3A23Z%22%7D%7D%2C%7B%22key%22%3A%22FJINQZDK%22%2C%22library%22%3A%7B%22id%22%3A858234%7D%2C%22meta%22%3A%7B%22creatorSummary%22%3A%22Zaimis%22%2C%22parsedDate%22%3A%221968-08%22%2C%22numChildren%22%3A1%7D%2C%22bib%22%3A%22%3Cdiv%20class%3D%5C%22csl-bib-body%5C%22%20style%3D%5C%22line-height%3A%201.35%3B%20%5C%22%3E%5Cn%20%20%3Cdiv%20class%3D%5C%22csl-entry%5C%22%20style%3D%5C%22clear%3A%20left%3B%20%5C%22%3E%5Cn%20%20%20%20%3Cdiv%20class%3D%5C%22csl-left-margin%5C%22%20style%3D%5C%22float%3A%20left%3B%20padding-right%3A%200.5em%3B%20text-align%3A%20right%3B%20width%3A%201em%3B%5C%22%3E1.%3C%5C%2Fdiv%3E%3Cdiv%20class%3D%5C%22csl-right-inline%5C%22%20style%3D%5C%22margin%3A%200%20.4em%200%201.5em%3B%5C%22%3EZaimis%20E.%20Vasopressor%20drugs%20and%20catecholamines.%20Anesthesiology.%201968%20Aug%3B29%284%29%3A732%26%23x2013%3B62.%3C%5C%2Fdiv%3E%5Cn%20%20%20%3C%5C%2Fdiv%3E%5Cn%3C%5C%2Fdiv%3E%22%2C%22data%22%3A%7B%22itemType%22%3A%22journalArticle%22%2C%22title%22%3A%22Vasopressor%20drugs%20and%20catecholamines%22%2C%22creators%22%3A%5B%7B%22creatorType%22%3A%22author%22%2C%22firstName%22%3A%22E.%22%2C%22lastName%22%3A%22Zaimis%22%7D%5D%2C%22abstractNote%22%3A%22%22%2C%22date%22%3A%221968%20Jul-Aug%22%2C%22language%22%3A%22eng%22%2C%22DOI%22%3A%22%22%2C%22ISSN%22%3A%220003-3022%22%2C%22url%22%3A%22%22%2C%22collections%22%3A%5B%228BC4ZE5V%22%5D%2C%22dateModified%22%3A%222017-08-07T06%3A36%3A47Z%22%7D%7D%2C%7B%22key%22%3A%222P7XKMMT%22%2C%22library%22%3A%7B%22id%22%3A858234%7D%2C%22meta%22%3A%7B%22creatorSummary%22%3A%22Smith%20and%20Corbascio%22%2C%22parsedDate%22%3A%221970-07%22%2C%22numChildren%22%3A1%7D%2C%22bib%22%3A%22%3Cdiv%20class%3D%5C%22csl-bib-body%5C%22%20style%3D%5C%22line-height%3A%201.35%3B%20%5C%22%3E%5Cn%20%20%3Cdiv%20class%3D%5C%22csl-entry%5C%22%20style%3D%5C%22clear%3A%20left%3B%20%5C%22%3E%5Cn%20%20%20%20%3Cdiv%20class%3D%5C%22csl-left-margin%5C%22%20style%3D%5C%22float%3A%20left%3B%20padding-right%3A%200.5em%3B%20text-align%3A%20right%3B%20width%3A%201em%3B%5C%22%3E1.%3C%5C%2Fdiv%3E%3Cdiv%20class%3D%5C%22csl-right-inline%5C%22%20style%3D%5C%22margin%3A%200%20.4em%200%201.5em%3B%5C%22%3ESmith%20NT%2C%20Corbascio%20AN.%20The%20use%20and%20misuse%20of%20pressor%20agents.%20Anesthesiology.%201970%20Jul%3B33%281%29%3A58%26%23x2013%3B101.%3C%5C%2Fdiv%3E%5Cn%20%20%20%3C%5C%2Fdiv%3E%5Cn%3C%5C%2Fdiv%3E%22%2C%22data%22%3A%7B%22itemType%22%3A%22journalArticle%22%2C%22title%22%3A%22The%20use%20and%20misuse%20of%20pressor%20agents%22%2C%22creators%22%3A%5B%7B%22creatorType%22%3A%22author%22%2C%22firstName%22%3A%22N.%20T.%22%2C%22lastName%22%3A%22Smith%22%7D%2C%7B%22creatorType%22%3A%22author%22%2C%22firstName%22%3A%22A.%20N.%22%2C%22lastName%22%3A%22Corbascio%22%7D%5D%2C%22abstractNote%22%3A%22%22%2C%22date%22%3A%22Jul%201970%22%2C%22language%22%3A%22eng%22%2C%22DOI%22%3A%22%22%2C%22ISSN%22%3A%220003-3022%22%2C%22url%22%3A%22%22%2C%22collections%22%3A%5B%228BC4ZE5V%22%5D%2C%22dateModified%22%3A%222017-08-07T06%3A36%3A25Z%22%7D%7D%5D%7D
1.
Mets B. Should Norepinephrine, Rather than Phenylephrine, Be Considered the Primary Vasopressor in Anesthetic Practice? Anesth Analg. 2016 May;122(5):1707–14.
1.
Ngan Kee WD, Lee SWY, Ng FF, Tan PE, Khaw KS. Randomized double-blinded comparison of norepinephrine and phenylephrine for maintenance of blood pressure during spinal anesthesia for cesarean delivery. Anesthesiology. 2015 Apr;122(4):736–45.
1.
DiNardo JA, Zvara DA. Anesthesia for Cardiac Surgery. John Wiley & Sons; 2008. 475 p.
1.
Magder S. Phenylephrine and tangible bias. Anesth Analg. 2011 Aug;113(2):211–3.
1.
Thiele RH, Nemergut EC, Lynch C. The clinical implications of isolated alpha(1) adrenergic stimulation. Anesth Analg. 2011 Aug;113(2):297–304.
1.
Kanaya N, Satoh H, Seki S, Nakayama M, Namiki A. Propofol anesthesia enhances the pressor response to intravenous ephedrine. Anesth Analg. 2002 May;94(5):1207–11, table of contents.
1.
Zaimis E. Vasopressor drugs and catecholamines. Anesthesiology. 1968 Aug;29(4):732–62.
1.
Smith NT, Corbascio AN. The use and misuse of pressor agents. Anesthesiology. 1970 Jul;33(1):58–101.




 Cette poche reste dans un endroit précis. De plus, j’ai plutôt tendance à faire de plus en plus de SAP. Les boli je les limite à 16 µg, quitte à les répéter (après un résultat de PNI) en attendant l’introduction de la SAP. Je me focalise sur les patients les plus âgés ou fragiles. La noradrénaline en bolus à un patient jeune, ASA 1, vierge de médicaments au long cours (anti-HTA, antidépresseurs, etc) me parait plus sujette à des réactions importantes. Autour de 30/40 ml/h, il faut réfléchir à la situation et il parait logique de préparer de la noradrénaline plus concentrée en SAP.
Cette poche reste dans un endroit précis. De plus, j’ai plutôt tendance à faire de plus en plus de SAP. Les boli je les limite à 16 µg, quitte à les répéter (après un résultat de PNI) en attendant l’introduction de la SAP. Je me focalise sur les patients les plus âgés ou fragiles. La noradrénaline en bolus à un patient jeune, ASA 1, vierge de médicaments au long cours (anti-HTA, antidépresseurs, etc) me parait plus sujette à des réactions importantes. Autour de 30/40 ml/h, il faut réfléchir à la situation et il parait logique de préparer de la noradrénaline plus concentrée en SAP.